
请使用微信扫描二维码登陆
"药原素网"


6.7万盒劣药流入市场
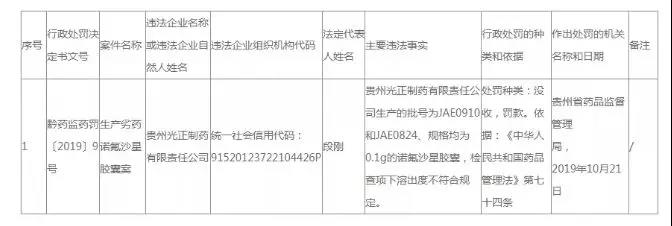
经查明,贵州光正制药有限责任公司共生产了批号为JAE0910的诺氟沙星胶囊39200盒,并全部销售完毕。随后该公司发现该批药溶出度下降幅度较大,为降低风险,于5月10日主动对该批药进行三级召回,且已于5月13日主动向贵州省药监局备案。截至7月23日,该批次诺氟沙星胶囊共召回9016盒,实际销售数量为30184盒,违法所得为64170.7元,货值金额为83840元。
批号为JAE0824的诺氟沙星胶囊共生产了40000盒,并全部销售完毕。该药企于5月10日主动对该批药进行三级召回,且已于5月13日主动向贵州省药监局备案。截至7月23日,该批次诺氟沙星胶囊共召回2901盒,实际销售数量为37099盒,违法所得为81617.8元,货值金额为88000元。
也就是说,贵州光正制药有限责任公司生产的这两批次不合规格诺氟沙星胶囊生产数量共计79200盒,实际销售67283盒,召回11917盒,两批次不合规格诺氟沙星胶囊违法所得共计人民币145788.5元,货值金额共计171840元。
据悉,2019年2月25日,遵义凤冈县市场监管局检查发现其辖区药品经营单位使用的诺氟沙星胶囊(批号为JAE0910、规格均为0.1g)不合格,不合格项目为溶出度。6月25日,贵州省药监局收到遵义不合格药品案件报告,并于当日去到贵州光正制药有限责任公司进行现场检查,同时送达检测检验报告。
7月2日,贵州光正制药有限责任公司向贵州省药监局递交复验申请。7月18日,贵州省药监局撤回其复验申请。
而在5月8日,遵义市市场监管局抽检中,再次发现该药企的诺氟沙星胶囊(批号为JAE0824、规格均为0.1g)不合格,并向贵州省药监局递交报告。贵州省药监局7月23日到该公司现场检查,发现该公司在规定时限内未提出复验申请。
依据《中华人民共和国药品管理法》第四十九条第三款第(六)项规定的“其他不符合药品标准规定”,贵州光正制药有限责任公司生产的批号为JAE0910和JAE0824、规格均为0.1g的诺氟沙星胶囊应当按劣药论处。
罚没款23.17万
贵州省药监局依据《中华人民共和国药品管理法》第七十四条(生产、销售假药的,没收违法生产、销售的药品和违法所得,并处违法生产、销售药品货值金额二倍以上五倍以下的罚款;有药品批准证明文件的予以撤销,并责令停产、停业整顿;情节严重的,吊销《药品生产许可证》、《药品经营许可证》或者《医疗机构制剂许可证》;构成犯罪的,依法追究刑事责任。)
同时,根据《中华人民共和国行政处罚法》第二十三条(行政机关实施行政处罚时,应当责令当事人改正或者限期改正违法行为的规定,决定责令贵州光正制药有限责任公司改正违法行为,并对贵州光正制药有限责任公司给予以下行政处罚:
1、没收劣药诺氟沙星胶囊11907盒;
2、没收违法所得共计人民币145788.5元;
3、处罚劣药诺氟沙星胶囊货值金额0.5倍的罚款共计人民币85920元。
以上罚没款共计人民币231708.5元。