请使用微信扫描二维码登陆
"药原素网"


随着生活水平提高、饮食结构和生活方式的改变,在过去的30年间全球糖尿病的患病率迅猛增长,据国际糖尿病联盟(IDF)2021年全球糖尿病概览第十版数据显示,2021年全球约5.37亿成年人(20-79岁)患有糖尿病,预计此后几年,这一数字还将持续攀升。
作为唯一能够降低血糖的激素,对于I型和Ⅱ型糖尿病人来说,胰岛素是维持生命的必备药品。但现有的胰岛素药品多为注射制剂,不易保存,用药难度较大,患者心理负担较大。于是,口服胰岛素成为人类的追求之一。
在尝试开发口服胰岛素时,纳米颗粒技术取得了重大的进展。纳米颗粒可以有效地封装和保护胰岛素不被降解,从而有针对性地输送到人体的特定部位。然而,纳米颗粒制剂的使用有一些限制,主要是由于颗粒悬浮液的稳定性问题。目前,冻干技术是创造稳定的NPs的黄金标准。但是,冻干技术需要添加冷冻保护剂,占据了大部分的重量比,这大大降低了冻干后胰岛素NPs的负载量。
在制药工业中,喷雾干燥是一种著名的、廉价的、从液相中生成干粉的工业规模的工艺。对颗粒形成过程的控制允许对几种生物活性化合物进行适当的封装。此外,它也是制备用于口服的封装蛋白质的一种有效技术。在喷雾干燥过程中,水的蒸发速度非常快,这有助于保持粒子核心的低温度,因此允许其应用于封装热敏成分。由于在喷雾干燥封装过程中不需要冷冻保护剂,因此,喷雾干燥可以用来生产具有高负荷含量的干燥NPs。
近日,The University of British Columbia的Anubhav Pratap-Singh团队在Scientific Reports上报道了通过使用电离凝胶法建立壳聚糖和三聚磷酸钠的交联来生产胰岛素负载NPs的过程。这项工作评估了冻干和喷雾干燥过程对负载胰岛素的壳聚糖纳米颗粒结构的影响。通过测量它们的尺寸分布、表面电荷、PDI、封装效率和装载量,评估了它们的重组能力。通过比较它们的胰岛素保护效果、释放行为和细胞摄取功效,也评估了不同脱水方法产生的再溶解纳米颗粒的质量。

图片来源:编译原文截图
研究表明,混合溶液的pH值以及壳聚糖和胰岛素的比例是影响最终NPs的颗粒大小和封装效率(EE)的两个关键因素,因为它们直接影响到离子凝胶过程。混合溶液的pH值被证明与颗粒大小和封装效率都有很高的关联(图1a)。此外,在壳聚糖/胰岛素质量比高于2.5:1(w/w)的情况下制备纳米颗粒时,EE没有变化(图1b)。因此,本研究中的最佳制备条件(pH6.0,壳聚糖/胰岛素质量比为2.5:1)被用来制备含有胰岛素的纳米颗粒,以进行进一步的研究。在这种制备条件下,胰岛素NPs的平均粒径被优化为318 nm(图1c),PDI为0.18,夹带效率为99.4%,Zeta电位为9.8 mv,胰岛素负载量为25.01%(m/m)。根据透射电子显微镜(TEM)的结果,优化后的纳米颗粒大致呈球形,离散,尺寸相对均匀(图1d)。
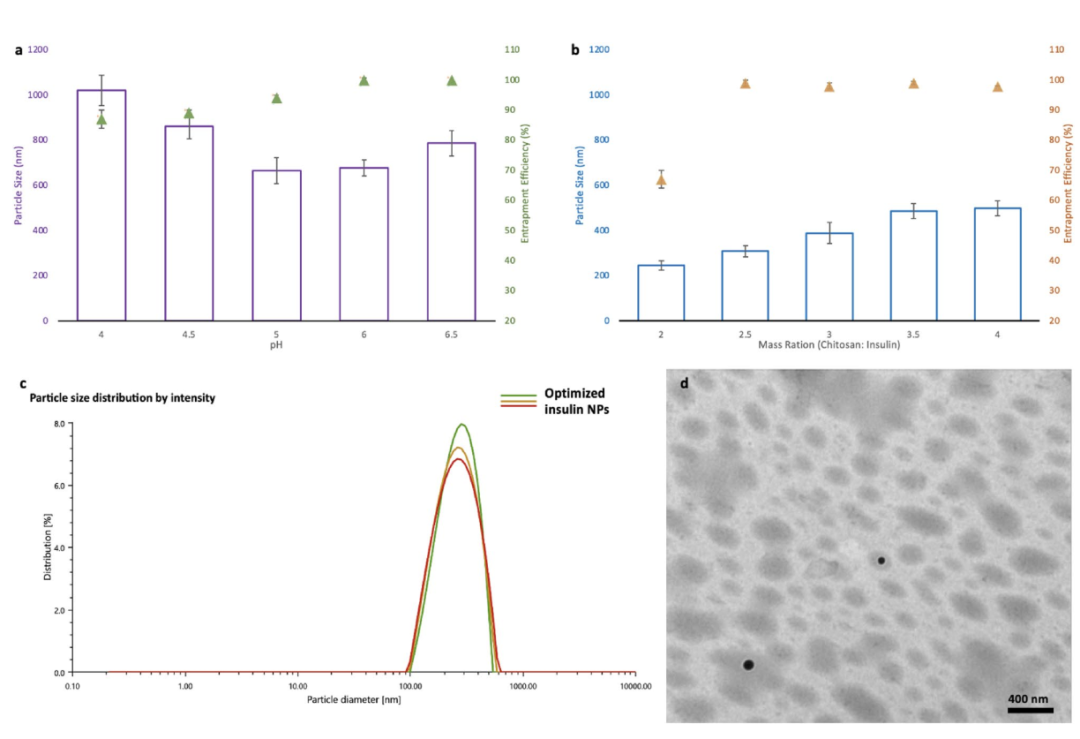
图1. 胰岛素NPs的参数优化:(a)pH值对胰岛素NPs平均直径和封装效率(EE)的影响(在壳聚糖和胰岛素的质量比为5:1的情况下制备);(b)壳聚糖和胰岛素的质量比对胰岛素NPs平均直径和封装效率(EE)的影响(在pH值为6时制备);(c)优化的胰岛素NPs的颗粒大小分布;(d)优化的胰岛素NPs的TEM显微照片。
(图片来源:Scientific Reports)
形态学分析表明,喷雾干燥可以使胰岛素纳米颗粒脱水而不需要冷冻保护剂,与传统的冷冻干燥方法相比,在提高装载能力、减少的添加剂要求和操作成本方面具有显著的优势。
对于不含甘露醇的冻干胰岛素NPs,如图2a所示,在扫描电子显微镜(SEM)下观察到一个高度多孔的粉末结构,表面大而不规则且粗糙。脱水后的粉末中几乎检测不到离散的颗粒(图2e)。
这些结果表明,在没有任何冷冻保护剂的情况下,大多数NPs在冻干过程中被分解了。对于含有1%甘露醇的冻干和喷雾干燥的胰岛素NPs,都观察到NPs呈球形,表面光滑(图2b, d, f, h)。不含甘露醇的胰岛素NPs喷雾干燥后保持其球形形状,但表面有皱纹(图2c)。根据干燥的NPs的可见外观,不含甘露醇的喷雾干燥NPs和冷冻干燥及含甘露醇的喷雾干燥NPs都形成了细小的NPs粉末(图2f,g,h)。微粒子表面之间更高的表面积会诱发更高的溶解度,因此,更高的释放率。
相比之下,在喷雾干燥过程中没有冷冻步骤。因此,在这种方法中,甘露醇是没有必要的。事实上,没有甘露醇的喷雾干燥NPs产生的NPs更细。然而,在喷雾干燥过程中,甘露醇仍可作为一种膨松剂,使NPs具有更多的球形结构(图2d),这有助于NPs的均匀释放胰岛素。本研究中,为了确保球形结构在脱水后能保持完整,甘露醇和壳聚糖的比例保持在5:1,这样大量的膨松剂也能扩大干燥NPs的颗粒尺寸。

图2. 不同脱水胰岛素NPs的形态。(a) 不含甘露醇的冻干胰岛素NPs的SEM图像;(b) 含甘露醇的冻干胰岛素NPs的SEM图像;(c) 不含甘露醇的喷雾干燥胰岛素NPs的SEM图像;(d)含甘露醇的喷雾干燥胰岛素NPs的SEM图像。(e) 不含甘露醇的冻干胰岛素NPs粉末的图像;(f) 含甘露醇的冻干胰岛素NPs的图像;(g) 不含甘露醇的喷雾干燥胰岛素NPs粉末的图像;(h) 含甘露醇的喷雾干燥胰岛素NPs的图像。
(图片来源:Scientific Reports)
在稳定性方面,所有的脱水NPs都在冰箱里保存了三个月。SEM结果表明,所有脱水NPs的形态在三个月的储存期间没有明显变化(图3)。

图3. 储存三个月的不同脱水胰岛素NPs的形态:(a)含甘露醇的冻干胰岛素NPs的SEM图像;(b)不含甘露醇的喷雾干燥胰岛素NPs的SEM图像;(c)不含甘露醇的喷雾干燥胰岛素NPs的SEM图像。
(图片来源:Scientific Reports)
随后,该研究评估了胰岛素NPs的释放效果。结果显示,游离胰岛素在所有三种酶处理中都显示出在4小时内快速消除胰岛素(图4a-c)。相比之下,用甘露醇冷冻干燥的NPs和用或不用甘露醇喷雾干燥的NPs的胰岛素消除试验显示,这些NPs对酶消化的保护作用明显较高,这与新鲜制备的胰岛素NPs相似(图4a-c)。这些结果表明,使用或不使用甘露醇的喷雾干燥和使用甘露醇的冷冻干燥可以保持NPs脱水后的胰岛素保护能力。
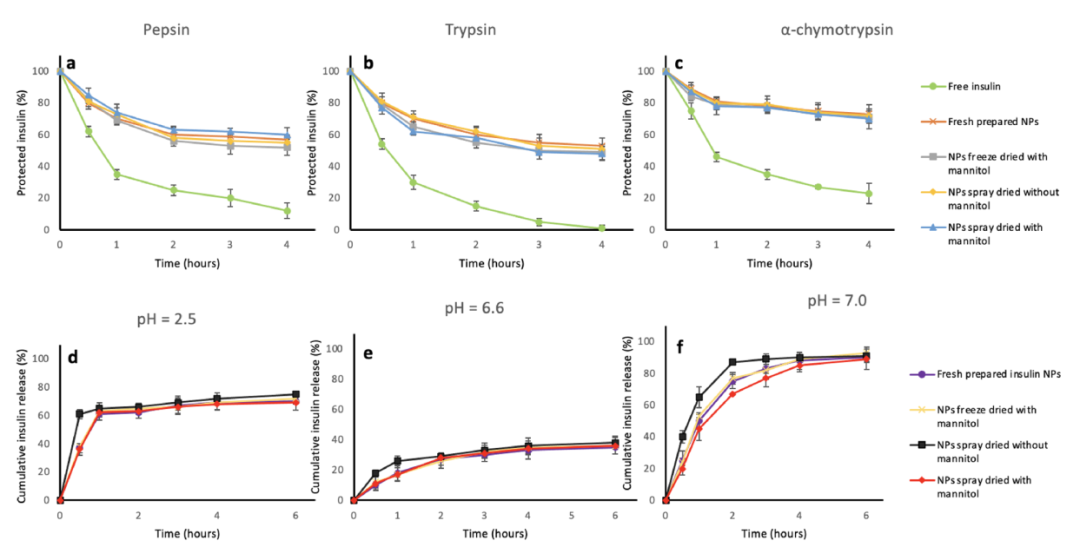
图4. 脱水胰岛素NPs的保护作用和释放行为:(a)胃蛋白酶溶液对胰岛素的保护;(b)胰蛋白酶溶液对胰岛素的保护;(c)α-糜蛋白酶溶液对胰岛素的保护;(d)脱水NPs在pH=2.5溶液中的释放行为;(e)脱水NPs在pH=6.6溶液中的释放行为;(f)脱水NPs在pH=7.0溶液中的释放行为。
(图片来源:Scientific Reports)
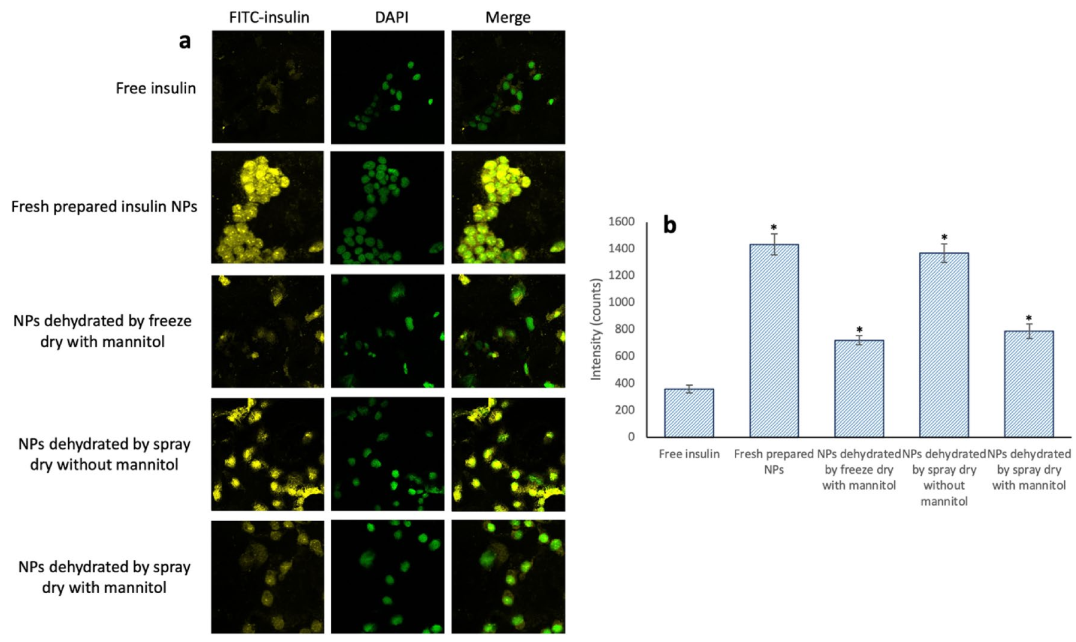
最后,HepG2细胞被用来评估采用冷冻干燥和喷雾干燥方法脱水的NPs的细胞吸收情况。结果表明,封装的胰岛素比游离的胰岛素在细胞吸收方面有更高的功效,这主要与研究中创建的胰岛素负载NPs的尺寸较小有关(图5)。